Technologia phage-display wykorzystuje bakteriofagi do prezentowania bibliotek peptydów, bądź białek na ich powierzchni. To narzędzia ma wiele zastosowań, w tym projektowanie nowych leków. Szczegóły tej technologii oraz zalet z nią związanych zostaną opisane w poniższym artykule.
Spis treści
Czym jest phage-display?
Phage display to technologia umożliwiająca ekspozycję peptydów, białek lub fragmentów przeciwciał na powierzchni bakteriofagów, przy jednoczesnym zachowaniu bezpośredniego związku między fenotypem a genotypem. Obca sekwencja DNA jest łączona z genem białka kapsydu, dzięki czemu po namnożeniu faga produkt fuzyjny zostaje wystawiony na jego powierzchni. Takie rozwiązanie pozwala tworzyć bardzo duże biblioteki wariantów i selekcjonować cząsteczki o pożądanym powinowactwie do określonego celu biologicznego [1]. Metoda została zapoczątkowana przez ekspozycję peptydu na białku pIII faga filamentującego [2], a następnie rozwinięta do selekcji przeciwciał i fragmentów przeciwciał [3].
Podstawy systemu filamentowego
Najczęściej stosowanym modelem jest fag M13 należący do grupy Ff. Jego kapsyd zawiera główne białko pVIII, obecne w około 2700 kopiach, oraz białko pIII, występujące w około 5 kopiach na końcu wirionu. pVIII sprzyja gęstej ekspozycji krótkich peptydów, natomiast pIII lepiej nadaje się do prezentacji większych peptydów, białek i fragmentów przeciwciał [Jaroszewicz, et al., 2022]. To rozróżnienie ma znaczenie praktyczne, ponieważ wpływa na walencję, awidność i charakter selekcji [1]. Schematyczny przykład wyglądu tego modelu jest pokazany na Ryc.1. i został zaczerpnięty z publikacji Jaroszewicz, et. al., [1].
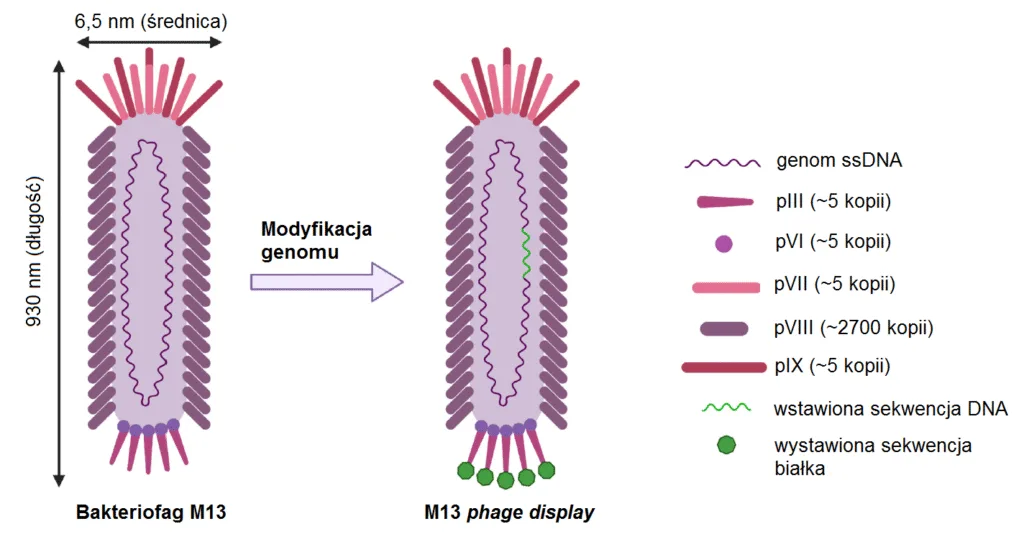
Bakteriofag M13 należy do filamentujących fagów, posiada jednoniciowy genom DNA, a jego kapsyd zbudowany jest z pięciu różnych białek. Technologia phage display polega na modyfikacji genomu faga poprzez wstawienie obcej sekwencji do genu białka kapsydu, co umożliwia prezentację obcego peptydu lub białka na powierzchni wirionu [Rycina z artykułu Jaroszewicz et. al., 2022, zmienione].
Format display i przebieg selekcji
Klasyczne systemy fagowe dają display poliwalentny, natomiast układy fagmidowe z fagiem pomocniczym umożliwiają display o niższej walencji, zwykle korzystniejszy przy izolacji silnych czynników wiążących [1]. Eksperyment obejmuje przygotowanie biblioteki, ekspozycję cząsteczek na powierzchni fagów, a następnie biopanning, czyli wiązanie do unieruchomionego celu, wypłukiwanie słabych interakcji, elucję związanych cząstek i ich amplifikację [1, 4]. Po kilku rundach uzyskuje się pulę wzbogaconą w klony swoiste, które identyfikuje się przez sekwencjonowanie [1].
Zalety i ograniczenia
Największą zaletą phage display jest możliwość przeszukiwania bibliotek o ogromnej liczebności przy niskim koszcie i stosunkowo prostej pracy laboratoryjnej. Technologia dobrze nadaje się do odkrywania ligandów, epitopów i przeciwciał, a także do inżynierii powinowactwa. Ograniczenia wynikają jednak z biologii fagów filamentowych: nie wszystkie białka poprawnie fałdują się w peryplazmie E. coli, duże lub hydrofobowe inserty mogą obniżać infekcyjność, a wysoka walencja może promować selekcję klonów o wysokiej awidności, lecz niekoniecznie najwyższym powinowactwie [1].
Inne platformy display
Aby obejść te ograniczenia, opracowano alternatywy wykorzystujące inne białka kapsydu fagów filamentowych, a także fagi T7, λ, T4, Qβ i MS2. Szczególnie systemy lityczne, takie jak T7 i T4, ułatwiają ekspozycję większych białek, ponieważ składanie wirionu zachodzi w cytoplazmie, a nie przez aparat sekrecyjny bakterii. Równolegle rozwinęły się bacterial display, yeast display, mammalian display oraz systemy bezkomórkowe, takie jak ribosome display i mRNA display. Każda z tych platform oferuje inny kompromis między wielkością biblioteki, jakością fałdowania białka i możliwością zachowania modyfikacji potranslacyjnych [1].
Zastosowania biologiczne i biomedyczne
Phage display i pokrewne technologie są dziś szeroko wykorzystywane w diagnostyce, projektowaniu leków, tworzeniu przeciwciał terapeutycznych, mapowaniu epitopów oraz badaniu interakcji białko-białko. Szczególne znaczenie mają biblioteki peptydowe i przeciwciał, zarówno immunizowane, jak i naiwne czy syntetyczne. Rozwój tych metod doprowadził już do powstania leków opartych na przeciwciałach wyselekcjonowanych z użyciem phage display, a integracja z sekwencjonowaniem nowej generacji dodatkowo zwiększyła rozdzielczość analizy selekcji [1].
Wnioski
Phage display pozostaje technologią niesamowicie przydatną dla nowoczesnej biologii molekularnej, ponieważ umożliwia funkcjonalną selekcję cząsteczek z ogromnych bibliotek i szybkie przejście od wiązania do identyfikacji sekwencji. Jednocześnie nie jest to system uniwersalny w sensie technicznym: jego skuteczność zależy od właściwego doboru platformy do rodzaju cząsteczki i celu badawczego. Rozwój kolejnych wariantów display pokazuje więc nie zastępowanie jednej metody przez drugą, lecz stopniowe budowanie komplementarnego zestawu narzędzi dla biologii, medycyny i biotechnologii.
Literatura
- Jaroszewicz, W., Morcinek-Orłowska, J., Pierzynowska, K., Gaffke, L., & Węgrzyn, G. (2022). Phage display and other peptide display technologies. FEMS microbiology reviews, 46(2), fuab052. DOI:10.1093/femsre/fuab052
- Smith, G. P. (1985). Filamentous fusion phage: novel expression vectors that display cloned antigens on the virion surface. Science, 228(4705), 1315-1317. DOI:10.1126/science.4001944
- McCafferty, J., Griffiths, A. D., Winter, G., & Chiswell, D. J. (1990). Phage antibodies: filamentous phage displaying antibody variable domains. nature, 348(6301), 552-554. DOI:10.1038/348552a0
- Parmley, S. F., & Smith, G. P. (1988). Antibody-selectable filamentous fd phage vectors: affinity purification of target genes. Gene, 73(2), 305-318. DOI:10.1016/0378-1119(88)90495-7
