Zarówno u bakterii Gram-dodatnich jak i Gram-ujemnych rozpowszechnione są enzymy, które prowadzą do chemicznej zmiany w cząsteczce antymikrobiologicznej. Do tej grupy zaliczają się enzymy modyfikujące aminoglikozydy (EMA) i acetylotransferazy chloramfenikolowe (CAT).
Spis treści
Modyfikacje enzymatyczne występujące w systemach oporności
Enzymy dokonujące chemicznych zmian w antybiotyku są skierowane głównie przeciw antybiotykom, które celują w hamowanie syntezy białek na poziomie rybosomów. Modyfikacje jakie tam występują to następująco:
- acetylacja (aminoglikozydy, chloramfenikol, streptograminy),
- fosforylacja (aminoglikozydy, chloramfenikol),
- adenylacja (aminoglikozydy, linkozamidy).
W nawiasach zostały podane niektóre antybiotyki, przeciw któremu dany mechanizm działania jest skierowany. Poza tym, że dochodzi do reakcji biochemicznej, to tworzy się jeszcze zawada przestrzenna przez co antybiotyk nie będzie tak chętnie wiązał się ze swoim celem (1, 2).
Enzymy modyfikujące aminoglikozydy
Wykorzystanie enzymów modyfikujących aminoglikozydy (EMA) wśród patogenów ESKAPE, to najpopularniejszy mechanizm oporności. Działają one poprzez kowalencyjną modyfikację grupy hydroksylowej bądź aminowej cząsteczki aminoglikozydu. Wykorzystują one 3 mechanizmy działania przez co można je podzielić na 3 różne klasy:
- acetylotransferazy aminoglikozydowe (AAC),
- fosfotransferazy aminoglikozydowe (APH),
- nukleotydylotransferazy (ANT).
Enzymy z każdej z tych klas są podzielone według pozycji miejsca modyfikacji (numery od 1 do 6 reprezentują numer węgla w pierścieniu cukrowym, a pojedynczy bądź podwójny apostrof oznacza kolejno pierwszą, albo drugą resztę cukrową w jakiej zachodzi reakcja), profilu oporności i specyficznego oznaczenia białka. Dodatkowo jeżeli daną reakcję katalizuje więcej niż jeden enzym, to dla ich rozróżnienia używa się rzymskiej numeracji (Ryc. 1) (1, 2, 3).
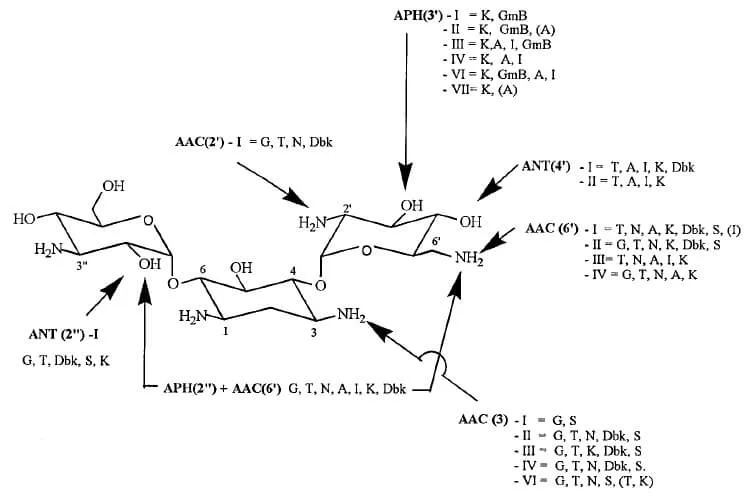
Geny kodujące EMA mogą być zlokalizowane najczęściej na plazmidach i transpozonach (mobilnych elementach genetycznych), a rzadziej na chromosomie (np. u Providencia stuartii, Enterococcus faecium, Serratia marcescens) (1, 2).
Przykłady występowania EMA i bifunkcjonalne enzymy
Istnieją pewne różnice w występowaniu oraz działaniu EMA na specyficzne aminoglikozydy u poszczególnych gatunków bakterii.
Przykład I: Rodzina APH(3) powszechnie występuje u bakterii Gram-dodatnich oraz Gram-ujemnych działając na kanamycynę i streptomycynę, natomiast nie wykazuje aktywności wobec gentamycyny i tobramycyny.
Przykład II: AAC(6′) występuje głównie u Gram-ujemnych izolatów klinicznych Enterobacteriacae, Pseudomonas i Acinetobacter działając na wiele aminoglikozydów.
Przykład III: Dystrybucja EMA z tej samej rodziny także może się różnić. Na przykład adenotytransferazy (działają na gentamycynę i tobramycynę) ANT(4′), ANT(6′) i ANT (9′) zwykle znajduje się na mobilnych elementach genetycznych bakterii Gram-dodatnich a ANT(2”) i ANT(3”) występują częściej u bakterii Gram-ujemnych.
Niektóre z tych enzymów posiadają więcej niż jedną biochemiczną aktywność. AAC(6′)APH(2”) głównie występuje u bakterii Gram-dodatnich i posiada aktywność acetylazy i fosfotrnsferazy. To białko prawdopodobnie powstało z fuzji dwóch genów. Odpowiada ono za wysoką oporność na niemal wszystkie aminoglikozydy, wyjątkiem jest streptomycyna. Obecność tego bifunkcjonalnego enzymu odpowiada za większość wysokiego poziomu oporności na gentamycynę u enterokoków (w tym wankomycynooporne) oraz gronkowców opornych na metycylinę (1, 2).
Acetylotransferazy chloramfenikolowe
To drugi kanoniczny przykład enzymów prowadzących do zmiany w antybiotyku. W tym przypadku dochodzi do modyfikacji w chlormafenikolu (który działa na podjednostkę 50S rybosomu) spowodowanej przez ekspresję genu cat, którego produktem jest acetylotransferaza chloramfenikolowa (CAT, Ryc.2) (1, 4).
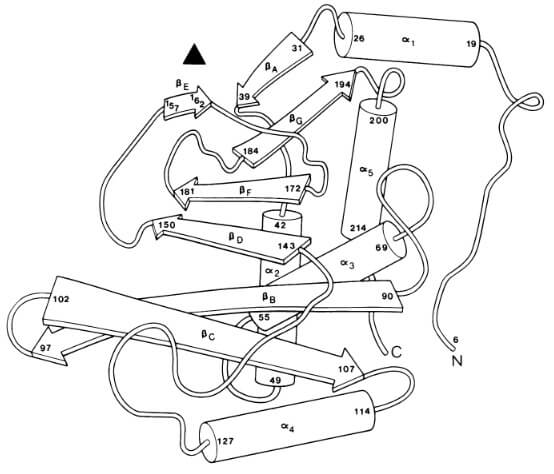
Geny cat znaleziono zarówno u bakterii Gram-dodatnich jak i Gram-ujemnych i dzieli się je na dwa główne typy:
- typ A – wysoka oporność na chloramfenikol,
- typ B – niska oporność na chloramfenikol.
Geny kodujące CAT zwykle znajduje się na mobilnych elementach genetycznych lecz u niektórych bakterii można je znaleźć także na chromosomie (1, 5).
Literatura
- Munita, J. M., & Arias, C. A. (2016). Mechanisms of antibiotic resistance. Virulence mechanisms of bacterial pathogens, 481-511. DOI: 10.1128/microbiolspec.VMBF-0016-2015.
- De Oliveira, D. M., Forde, B. M., Kidd, T. J., Harris, P. N., Schembri, M. A., Beatson, S. A., … & Walker, M. J. (2020). Antimicrobial resistance in ESKAPE pathogens. Clinical microbiology reviews, 33(3), e00181-19. DOI: https://doi.org/10.1128/CMR.00181-19.
- Mingeot-Leclercq, M. P., Glupczynski, Y., & Tulkens, P. M. (1999). Aminoglycosides: activity and resistance. Antimicrobial agents and chemotherapy, 43(4), 727-737. DOI:10.1128/aac.43.4.727.
- Leslie, A. G., Moody, P. C., & Shaw, W. (1988). Structure of chloramphenicol acetyltransferase at 1.75-A resolution. Proceedings of the National Academy of Sciences, 85(12), 4133-4137. DOI: 10.1073/pnas.85.12.4133
- Bale, B. I., Elebesunu, E. E., Manikavasagar, P., Agwuna, F. O., Ogunkola, I. O., Sow, A. U., & Lucero-Prisno, D. E. (2023). Antibiotic resistance in ocular bacterial infections: an integrative review of ophthalmic chloramphenicol. Tropical medicine and health, 51(1), 1-10. DOI: 10.1186/s41182-023-00496-x.
.
