Już wiemy jak działają pompy efflux oraz zmniejszenie przepuszczalności błony. W tej części skupimy się na takim mechanizmie oporności bakterii, jak inaktywacja antybiotyku. Ten typ oporności jest szeroko rozpowszechniony i został wykryty niedługo po odkryciu penicyliny.
Spis treści
Inaktywacja antybiotyku
Może do niej dojść poprzez działanie enzymu, który:
- niszczy miejsce aktywne antybiotyku,
- albo modyfikuje ważne elementy strukturalne leku, co utrudnia interakcję z celowaną strukturą znajdującą się w bakterii (na tym skupimy się w kolejnym artykule).
Zniszczenie cząsteczki antybiotyku
Enzymy, które zostały odkryte niedługo po znalezieniu penicyliny to beta-laktamazy. Geny kodujące te enzymy nazywa się bla po czym występuje nazwa konkretnego enzymu, np. blaIMP. Niszczą one wiązanie amidowe w pierścieniu Beta-laktamowym, co czyni antybiotyk nieefektywnym w działaniu antymikrobiologicznym. Są one szeroką grupą enzymów, która stanowi poważne źródło oporności wśród patogenów ESKAPE, u których kumulują się w peryplazmie.
Białko wiążące peptydoglikan (PBP) jest ważnym elementem biorącym udział w syntezie ściany komórkowej, jednak do pełnej syntezy są potrzebne także inne czynniki. Beta-laktamazy hydrolizują je zanim dotrą do PBP.
Beta-laktamazy można sklasyfikować w oparciu o dwa schematy. Klasyfikacja Amblera (Ryc. 1) opiera się na podobieństwie aminokwasowym i dzieli te enzymy na 4 grupy (A, B, C, D). Druga klasyfikacja, Blush-Jacoby’ego, dzieli Beta-laktamazy na 4 kategorie, z czego każda podzielona jest na podgrupy, a podział opiera się o ich funkcję biochemiczną.
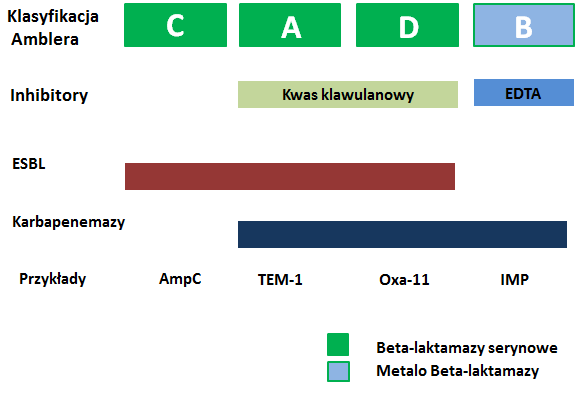
Podział Beta-laktamaz według Amblera
Klasa A
Enzymy klasy A to największa grupa enzymów Beta-laktamaz zdolna do inaktywacji większości klas Beta-laktamów. Zawierają serynę w centrum aktywnym (tak jak klasa C i D) i obejmują: penicylinazy, cefalosporynazy, Beta-laktamazy o wąskim i o szerokim spektrum, Beta-laktamazy o rozszerzonym spektrum (ESBL – extended spectrum Beta-lactamases) i karbapenemazy. Większość enzymów tej klasy może być inaktywowana kwasem klawulanowym.
CTX-M jest enzymem ESBL kodowanym na plazmidzie i często znajduje się go w bakteriach Klebsiella pneumoniae, Escherichia coli a także u innych Enterobacteriacae. Enzymy CTX-M najpowszechniejszymi ESBL i są odpowiedzialne za dużą część oporności jaka występuje u K. pneumoanie i E. coli.
Do dziś zidentyfikowano 5 rodzin karbapenemaz klasy A z czego 3 kodowane są na chromosomie a 2 pozostałe przenoszone są na plazmidach bądź innych mobilnych elementach genetycznych (MGE – mobile genetics elements). KPC to jedna z rodzin karbapenemaz kodowana na MGE i pierwszy zgłoszony przypadek miał miejsce w 1996 roku w Północnej Karolinie, w Stanach Zjednoczonych u pacjenta, od którego wyizolowano K. pneumoniae. Później też znajdowano KPC w innych Klebsiella spp. (stąd nazwa KPC – Klebsiella pneumoniae carbapenemase).
Klasa B
Klasa B nazywana jest również metalo-Beta-laktamazami ze względu na to, że jako kofaktor używają jonu metalu do nukleofilowego ataku na pierścień Beta-laktamowy. Można je inaktywować dzięki dodaniu chelatora, np. EDTA. Są aktywne wobec szerokiego spektrum Beta-laktamów, także na karbapenemy.
W latach dziewięćdziesiątych XX wieku te enzymy były powszechnie rozpoznawane w szczepach klinicznych Eneterobaceriacae, Pseudomonas spp. i Acinetobacter spp. Wyróżniemy około 10 rodzin metalo-karbapenemaz, z czego 4 są klinicznie istotne: IMP, VIM, SPM i NDM.
Warto wiedzieć, że MGE, na których kodowane są enzymy NDM zwykle zawierają także geny kodujące inne czynniki oporności takie jak: karbapenemazy, ESBL, białko Qnr (oporność na chinolony), enzymy modyfikujące rifampicynę i wiele innych. W związku w tym obecność NDM-1 jest zwykle fenotypowana wielolekoopornościowo.
Klasa C
Klasa C Beta-laktamaz odpowiada za oporność na penicyliny i cefalosporyny. Znanym enzymem z tej klasy jest AmpC, czyli cefalosporynaza kodowana na chromosomie (chociaż obserwuje się geny kodujące AmpC także na plazmidach). Produkcja chromosomowego AmpC jest typowa dla takich bakterii jak: Enterobacter cloacae, E. aerogenes, Clostridium freundii, S. marcescens, Providencia sp., Morganella morgrani, P. aeruginosa.
Klasa D
To Beta-laktamazy, w których skład wchodzi szerokie spektrum enzymów. Początkowo różniły się one od penicylinaz klasy A zdolnością do hydrolizy oksacyliny oraz dlatego, że kwas klawulanowy wykazywał niewielki efekt hamujący wobec tych enzymów.
Podsumowując, mechanizmy oporności można podzielić na wiele grup i rodzin według różnych klasyfikacji. To co można zaobserwować, to poziom zaawansowania ewolucji bakterii do zdolności wykształcania oporności. Jako ludzie musimy rozsądnie postępować z antybiotykami, bo jak widać, wciąż szukamy lepszych i skutecznych rozwiązań do walki z bakteriami.
Literatura:
- Munita, J. M., & Arias, C. A. (2016). Mechanisms of antibiotic resistance. Virulence mechanisms of bacterial pathogens, 481-511. DOI: 10.1128/microbiolspec.VMBF-0016-2015.
- De Oliveira, D. M., Forde, B. M., Kidd, T. J., Harris, P. N., Schembri, M. A., Beatson, S. A., … & Walker, M. J. (2020). Antimicrobial resistance in ESKAPE pathogens. Clinical microbiology reviews, 33(3), e00181-19. DOI: https://doi.org/10.1128/CMR.00181-19.
Oba artykuły naukowe zostały naprzemiennie wykorzystane w całym tekście.
