Biofilm to zwarta i uporządkowana grupa mikroorganizmów, która swój rozwój zaczyna od przyłączenia do powierzchni biotycznych bądź abiotycznych i rośnie w wytwarzanej przez siebie macierzy pozakomórkowej. W takiej społeczności drobnoustroje wykazują różny poziom rozwoju. Jest to jeszcze jeden mechanizm obronny bakterii, w tym oporności na antybiotyki. Przybliżymy sobie zjawisko powstawania biofilmu, wyjaśnimy czym są komórki przetrwałe i czym jest zjawisko quorum sensing.
Spis treści
Dlaczego biofilm bakteryjny jest niebezpieczny
Biofilmy bakteryjne są 1000 razy bardziej oporne na antybiotyki niż bakterie w formie planktonicznej (w płynie). Ich oporność wiąże się także z obecnością komórek przetrwałych, których znaczenie też wyjaśnimy. Struktura ta występuje w różnych środowiskach, na różnych powierzchniach począwszy od naszych tkanek, po narzędzia np. chirurgiczne, kanały wodne, toalety, podłogi, jednostki przetwarzające żywność. Biofilm może powstać wszędzie. W zależności od etapu rozwoju biofilmu, tego jakie geny w danym momencie uległy ekspresji, co wiąże się z aktywnością metaboliczną bakterii ich oporność będzie się różnić [1]. Dane Narodowego Instytutu Zdrowia USA pokazują, że 65% wszystkich chorób o podłożu bakteryjnym i 80% przewlekłych infekcji spowodowanych jest przez biofilmy. Jest to zmora szpitali, personelu medycznego i pacjentów [2].
Biofilm może utworzyć się na przykład na kamieniach nerkowych [3]. W przypadku rozbijania kamieni bakterie mogą się przedostać do krwiobiegu i wywołać sepsę. Pacjenci, którzy używają cewnika też są narażeni na infekcje bateryjne przy niezachowaniu odpowiednich zasad higieny, ponieważ biofilm łatwo tworzy się w cewniku [4].
Wyżej podane przykłady dotyczą medycyny, albo biofilm często pojawia się także w przemyśle spożywczym [5]. Można tak wymieniać w nieskończoność, ponieważ istnieje wiele takich przykładów, gdzie tworzą się biofilmy bakteryjne i jakie to niesie za sobą konsekwencje.
Jak powstaje biofilm
Zacznijmy od tego, że biofilm może tworzyć jeden szczep bakteryjny, albo może być to kultura mieszana. Niezależnie od tego, jakie bakterie wchodzą w skład biofilmu, to powstaje on w ten sam sposób. W ostawaniu biofilmu można wyróżnić 4 główne kroki:
- przyłączenie się komórek do powierzchni,
- formowanie mikrokolonii i wzrost,
- dojrzewanie biofilmu,
- oderwanie się komórek, by rozpocząć cykl od początku [6].
Cały schemat powstawania biofilmu przedstawiony jest na Ryc. 1.
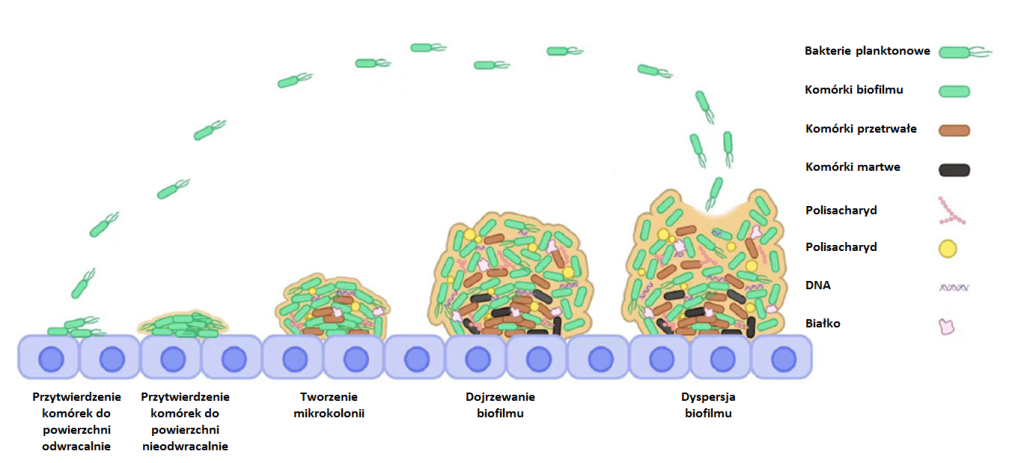
Przyłączenie się komórek do powierzchni
Na początku komórki bakteryjne przyłączają się do danej powierzchni w sposób odwracalny. Następnie zmieniają swoją orientację i zostają przytwierdzone w sposób nieodwracalny. Zjawisku temu towarzyszy zwiększona produkcja cząsteczki sygnałowej Bis-(3ʹ-5ʹ)-cyklicznego dimerycznego guanozynomonofosforanu (c-di-GMP). Odpowiada ona za zmniejszenie ruchliwości wici i zwiększenia produkcji macierzy biofilmu [1, 7].
Formowanie się mikrokolonii
Następnie bakterie zaczynają się namnażać i agregować wewnątrz macierzy pozakomórkowej substancji polimerycznej (EPS), którą produkują tworząc mikrokolonię z wysokim stężeniem c-di-GMP Flagella odpowiedzialne są tutaj za interakcje między mikroorganizmami a powierzchnią a typ IV pili umożliwia agregację i tworzenia mikrokolonii.
EPS stanowi ważny czynnik rozwoju biofilmu a poza tym jest bogaty w białka i struktury białkowe. W samej macierzy biofilmu obecne są także lipidy i DNA [1, 7].
Dojrzewanie biofilmu
Wraz z podziałem komórek bakterii tworzy się trójwymiarowa struktura. Zachodzą zmiany w ekspresji genów i tworzy się macierz biofilmu. EPS bardzo dobrze chroni komórki bakteryjne przez stresem zewnętrznym, np. układem odpornościowym gospodarza, czy antybiotykami. Po utworzeniu macierzy powstają struktury, takie jak kanały wodne, które umożliwiają transport substancji do społeczności bakterii. Ważną rolę w komunikacji bakterii odgrywa tutaj zjawisko quorum-sensing [1, 7]. To zjawisko zostanie szczegółowo omówione w osobnych artykule.
Odrywanie się biofilmu
Dojrzały biofilm składa się z trzech warstw: wewnętrznej regulującej, środkowej warstwy podłoża drobnoustrojów i zewnętrzna zamieszkała przez komórki planktonowe gotowe do opuszczenia biofilmu. To jest finalny stan rozwijającego się biofilmu. Dojrzały biofilm ulega częściowemu zniszczeniu, dalej się buduje, ale oderwane komórki mogą zasiedlić nową przestrzeń i zacząć tworzenie biofilmu od nowa [1, 7].
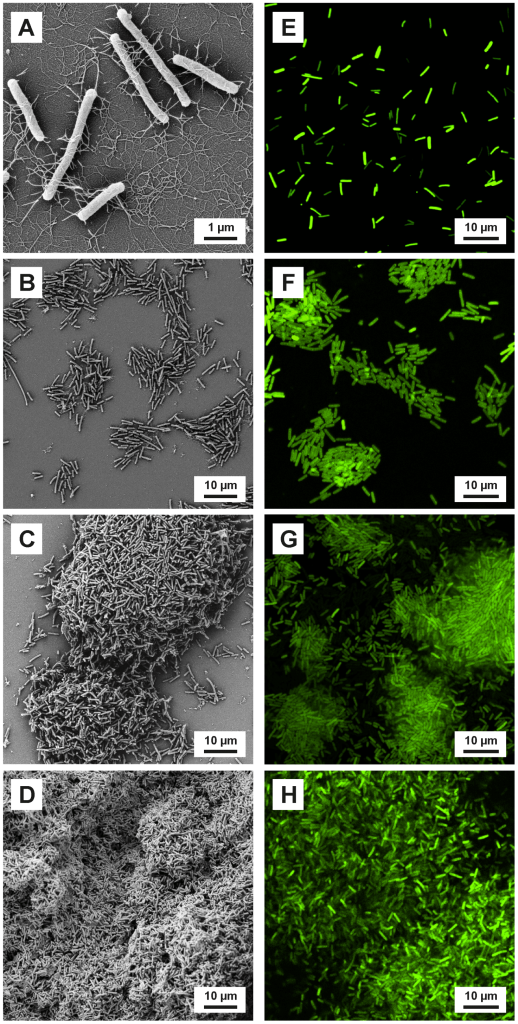
Wszystkie z tych etapów są zaprezentowane też na Ryc. 2., gdzie widzimy zdjęcia, jakie wykonała grupa Claudii Lüdecke, et. al .[8].
Kompozycja biofilmu
Biofilm składa się z:
- komórek bakteryjnych (2-5%)
- egzopolisacharydu (1-2%) – utrzymuje strukturę i stabilizuje macierz biofilmu,
- białek, wliczając w to enzymy (<1-2%) – utrzymują stabilność macierzy biofilmu i kolonizację powierzchni a poza tym odpowiadają za jego integralność,
- zewnątrz-komórkowego DNA (<1-2%) – promuje formowanie biofilmu, chroni jego integralność, utrzymuje stabilność struktury i chroni przed systemem obronnym gospodarza,
- wody (do 97%) – utrzymuje nawodnienie biofilmu zapobiegając wyschnięciu [1, 7]
Komórki przetrwałe
W biofilmach znaleźć można subpopulację komórek, które są nieaktywne i większość antybiotyków jest nieefektywna w walce z nimi. Są to tak zwane komórki przetrwale (ang. persister cells), które stanowią rezerwuar choroby, mogą uaktywnić się po zniknięciu ze środowiska czynnika stresowego [1].
Zjawisko Quorum sensing
Quorum sensing jest wewnątrz-komórkowym sposobem komunikacji bakterii, który odpowiada za wyczuwanie gętości biofilmu poprzez cząsteczki sygnałowe takie jak laktony N-acylohomoseryny (AHL), autoindukujący peptyd (AIP) i autoinduktor-2 (AI-2). Systemy działania quorum sensing są dobrze poznane m. in. w bakteriach Pseudomonas aeruginosa, gdzie działają ich 4 rodzaje [1].
Metody zwalczania biofilmu
Najbardziej tradycyjnym i chyba jak dotąd najskuteczniejszym sposobem usuwania biofilmu jest jego mechaniczne usuwanie. Jednak nie wszędzie da się to zrobić. Wyobrażacie sobie szczotkowanie czegoś w środku organizmu? No właśnie, jest to niemożliwe.
Eradykacja biofilmu, to kolejne wyzwanie jakie przed nami stoi w dobie lekooporności bakterii. W związku z tym naukowcy szukają alternatyw i badają zwalczanie biofilmu poprzez:
- bakteriofagi,
- inhibitory quorum sensing,
- peptydy antybakteryjne,
- enzymy,
- EDTA,
- nanocząstki,
- metabolity wtórne roślin,
- olejki eteryczne,
- zastosowanie metod fotodynamicznych i elektrochemicznych.
Wiele z tych pomysłów jest obiecujących i miejmy nadzieję, że dalsze badania nad tym będą rozwijane i wprowadzane w życie [9].
Literatura
- Rather, M. A., Gupta, K., & Mandal, M. (2021). Microbial biofilm: formation, architecture, antibiotic resistance, and control strategies. Brazilian Journal of Microbiology, 1-18. DOI:10.1007/s42770-021-00624-x
- Zafer, M. M., Mohamed, G. A., Ibrahim, S. R., Ghosh, S., Bornman, C., & Elfaky, M. A. (2024). Biofilm-mediated infections by multidrug-resistant microbes: A comprehensive exploration and forward perspectives. Archives of Microbiology, 206(3), 101. DOI:10.1007/s00203-023-03826-z.
- Wan, W., Wu, W., Amier, Y., Li, X., Yang, J., Huang, Y., … & Yu, X. (2024). Engineered microorganisms: A new direction in kidney stone prevention and treatment. Synthetic and Systems Biotechnology. DOI:10.1016/j.synbio.2024.02.005
- So, B., Kim, J., Jo, J. K., & So, H. (2024). Recent developments in preventing catheter-related infections based on biofilms: A comprehensive review. Biomicrofluidics, 18(5). DOI:10.1063/5.0195165.
- Alonso, V. P. P., Gonçalves, M. P. M., de Brito, F. A. E., Barboza, G. R., Rocha, L. D. O., & Silva, N. C. C. (2023). Dry surface biofilms in the food processing industry: An overview on surface characteristics, adhesion and biofilm formation, detection of biofilms, and dry sanitization methods. Comprehensive Reviews in Food Science and Food Safety, 22(1), 688-713. DOI:10.1111/1541-4337.13089.
- Rabin, N., Zheng, Y., Opoku-Temeng, C., Du, Y., Bonsu, E., & Sintim, H. O. (2015). Biofilm formation mechanisms and targets for developing antibiofilm agents. Future medicinal chemistry, 7(4), 493-512. DOI:10.4155/fmc.15.6.
- Zhao, A., Sun, J., & Liu, Y. (2023). Understanding bacterial biofilms: From definition to treatment strategies. Frontiers in cellular and infection microbiology, 13, 1137947. DOI:10.3389/fcimb.2023.1137947.
- Claudia Lüdecke, Klaus D. Jandt , Daniel Siegismund, Marian J. Kujau, Emerson Zang, Markus Rettenmayr, Jörg Bossert, Martin Roth (2014). Reproducible Biofilm Cultivation of Chemostat-Grown Escherichia coli and Investigation of Bacterial Adhesion on Biomaterials Using a Non-Constant-Depth Film Fermenter. PLoS One 9(1), e84837. DOI:10.1371/journal.pone.0084837.
- Srivastava, A., Verma, N., Kumar, V., Apoorva, P., & Agarwal, V. (2024). Biofilm inhibition/eradication: exploring strategies and confronting challenges in combatting biofilm. Archives of Microbiology, 206(5), 212. DOI:10.1007/s00203-024-03938-0.
