Przy opisie budowy ściany komórkowej bakterii mówiliśmy, że możemy je podzielić na Gram-dodatnie
i Gram-ujemne. Wiemy już czym jest barwienie Grama i znamy pojedyncze kroki, które pozwolą nam na wybarwienie komórek. Dziś omówimy etapy tego barwienia, ale najpierw krótko przybliżymy historię jego powstania.
Spis treści
Historia barwienia Grama
Hans Christian Gram w 1814 r. chciał zwizualizować ziarniaki, które były obecne w tkance płucnej osób zmarłych na zapalenie płuc. Wiedział już, że Robert Koch barwił fioletem krystalicznym (barwnik znany też pod nazwą gencjana) bakterie Mycobacterium tuberculosis. Gram nie chciał barwić komórek eukariotycznych, więc po użyciu fioletu dodał jodynę. Jod z fioletem krystalicznym tworzy kompleksy. Później do odbarwienia użył etanolu. Przestrzenie między warstwami peptydoglikanu obkurczyły się, barwnik nie wydostał się z komórek bakteryjnych i można je było zaobserwować pod mikroskopem świetlnym. W międzyczasie Gram zauważył, że pałeczki Salmonella Typhimurium nie zabarwiają się [1]. My dziś już wiemy, że są to bakterie Gram ujemne i żeby je zabarwić trzeba użyć dodatkowego barwnika.
Barwienie Grama
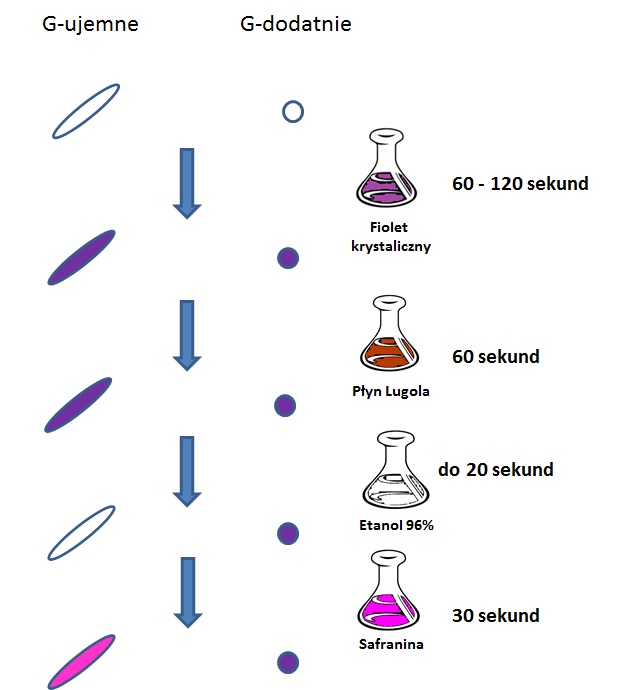
Barwienie Grama polega na wybarwieniu komórek bakteryjnych barwnikami, które pozwolą na odróżnienie ich od siebie pod mikroskopem świetlnym. Schemat barwienia wygląda jak na Ryc. 1 a poniżej wypisane są poszczególne kroki:
- barwienie we fiolecie krystalicznym,
- barwienie w płynie Lugola,
- odbarwianie alkoholem,
- barwienie dodatkowym barwnikiem, np. safraniną.
Po każdym z etapów nadmiar barwnika bądź rozpuszczalnika przepłukujemy wodą. Robimy to delikatnie, nad naniesionymi bakteriami, aby nie spłukać ich ze szkiełka. Poniżej wyjaśnimy sobie jakie znaczenie odgrywają poszczególne kroki barwienia.
Utrwalenie preparatu do barwienia
Zanim zaczniemy barwić preparat jakąkolwiek metodą, to musimy nanieść go na szkiełko podstawowe. Najpierw nanosimy kroplę 0,85% NaCl (sól fizjologiczna), czyli około 30-50 μL a następnie za pomocą ezy nanosimy 1 kolonię bakteryjną. Bakterie mieszamy w soli pokrywając około 1/3 powierzchni szkiełka. Preparat nie może być zbyt gęsty, ponieważ utrudni nam to późniejszą obserwację bakterii pod mikroskopem. Następnie przechodzimy do utrwalenia preparatu. W tym momencie unosimy szkiełko nad płomień i kilkukrotnie, z kilku-sekundowymi przerwami, przenosimy je nad płomieniem. Nie możemy doprowadzić do przegrzania szkiełka, bo w konsekwencji możemy „spalić” nasze bakterie. W momencie, gdy preparat jest suchy możemy zabrać się za barwienie właściwe.
Barwienie fioletem krystalicznym
Preparat umieszczamy w roztworze fioletu krystalicznego na 1 minutę, a następnie nadmiar spłukujemy pod delikatnym strumieniem wody. Fiolet przechodzi między warstwy peptydoglikanu, gdzie się zatrzymuje [1].
Barwienie płynem Lugola
Płyn Lugola jest wodnym roztworem jodku potasu. Preparat umieszcza się w takim roztworze na około 1 minutę, a nadmiar spłukuje wodą. Jod z fioletem krystalicznym tworzy kompleksy, przez co później barwnik nie może odpłukać się z komórek Gram-dodatnich, gdzie warstwa peptydoglikanu jest grubsza [2, 3].
Odbarwianie alkoholem
Następnym krokiem jest odbarwienie preparatu alkoholem. Barwnik wypłucze się z bakterii Gram-ujemnych, ponieważ doprowadza do rozpuszczenia lipidów budujących zewnętrzną błonę komórkową
i wydostanie się z cienkiej warstwy peptydoglikanu. W przypadku bakterii Gram-dodatnich barwnik zostanie. Dzieje się tak dlatego, że po pierwsze alkohol działa odwadniająco a po drugie barwnik z jodem tworzą na tyle duże kompleksy, iż nie jest w stanie wydostać się poza ścianę komórkową [1, 2, 3]. Na schemacie (Ryc. 1) pokazano odbarwianie etanolem, które trwa do około 20 sekund. Można też to zrobić za pomocą acetonu i wtedy maksymalny czas spłukiwania wynosi 10 sekund. Zbyt długi czas spłukiwania może doprowadzić do tego, że bakterie Gram-dodatnie także mogą się odbarwić [2].
Barwienie dodatkowym barwnikiem
Bakterie Gram-dodatnie są zabarwione na fioletowo ze względu na fiolet krystaliczny. Natomiast bakterie Gram-ujemne zostały odbarwione alkoholem i aby móc je obserwować pod mikroskopem należy dodać inny barwnik. W tym celu często wykorzystuje się safraninę, albo fuksynę zasadową. Zabarwi ona komórki bakterii G-ujemne na różowo, co nie wpłynie na zabarwienie komórek G-dodatnich. Nadmiar barwinka delikatnie spłukuje się wodą a potem preparat musi wyschnąć (nadmiar wody można też delikatnie odsączyć bibułką) i preparat jest gotowy do oglądania [1, 2].
Zjawisko Gram-chwiejności
Wiek kultury bakteryjnej jaką oglądamy pod mikroskopem ma znaczenie. Bakterie powinny znajdować się w logarytmicznej fazie wzrostu. Wynik barwienia starszych bakterii może być zafałszowany ze względu na degradację ściany komórkowej. Są też bakterie, które są szczególnie podatne na zjawisko Gram-chwiejności a to m. in. bakterie z rodzaju Bacillus, czy Clostridium [1, 2].
Niektóre baterie też nie barwią się według typu ściany komórkowej, np. bakterie z rodzaju Acinetobacter są Gram-negatywne, ale alkohol nie powoduje ich odbarwienia i pod mikroskopem są fioletowe [1].
Literatura
- Ann C. Smith, Marise A. Hussey (2005). Gram Stain Protocols. AmericanSociety for Microbiology.
- Moyes, R. B., Reynolds, J., & Breakwell, D. P. (2009). Differential staining of bacteria: gram stain. Current Protocols in Microbiology, 15(1), A-3C. DOI: 10.1002/9780471729259.mca03cs15.
- Beveridge, T. J., & Davies, J. A. (1983). Cellular responses of Bacillus subtilis and Escherichia coli to the Gram stain. Journal of bacteriology, 156(2), 846-858. DOI: 10.1128/jb.156.2.846-858.19.
