W dobie narastającej oporności na antybiotyki biobanki fagowe spełniają istotną rolę w rozwoju terapii fagowej. Biobanki fagów, to w obecnej formie pasywne magazyny próbek, zbierane lokalnie stanowiąc głównie część danego projektu, chociaż niekóre instytucje, jak Instytut Immunologi i Terapii Doświadczalnej im. Ludwika Hirszfelda we Wrocławiu posiadają swój stały bank wciąż poszerzany o nowe izolaty fagowe. W tym artykule omówimy ówczesny wygląd biobanków i przedyskutujemy wizje, jak powinien on wyglądać, by móc efektywnie wspierać całą infrastrukturę zdrowia publicznego.
Spis treści
Ogólny opis biobanków fagów
Biobanki fagów określa się jako repozytoria fagów. Aktualnie terapia fagowa polega na strategiach ad hoc, a w tym izolację fagów na zamówienie, nieformalną wymianę między laboratoriami lub sieci pomocy w sytuacjach nadzwyczajnych (zastosowanie ze względów humanitarnych) [1]. Są to osobne struktury, które działają jak kolekcje. Zanim opowiemy sobie, jak takie banki powinny działać, to najpierw skupimy się na przeszłości dotyczącej pierwszych kolekcji mikroorganizmów.
Jak to działa?
Opisane przypadki działania banku fagów są oparte na przykładzie belgisjkiego podejścia, gdzie terapię fagową wykorzystuje się jako alternatywna metoda leczenia dla antybiotyków.
Działanie zintegrowanego banku fagów opiera się na modelu, który koordynuje proces od izolacji po terapię. Po pobraniu próbki następuje jej standaryzacja: fagi są izolowane, oczyszczane i charakteryzowane zgodnie z rygorystycznymi protokołami (np. ISO 9001). Kluczowym etapem jest nadanie im tzw. Paszportu Faga, czyli cyfrowej dokumentacji zawierającej dane o genomie, nomenklaturze i spektrum gospodarzy, powiązanej z systemami nadzoru bakteriologicznego. Dane te trafiają do systemu umożliwiając szybkie wyszukiwanie preparatów. Następnie, w ramach diagnostyki towarzyszącej, specjaliści dopasowują fagi do konkretnych patogenów, badając synergię z antybiotykami. Ostatnim etapem jest bioprocesowanie (często klasy GMP), które dostarcza ultra-czyste preparaty do użytku klinicznego, przy jednoczesnym monitorowaniu odpowiedzi pacjenta [5]. Uproszczony pipeline takiej procedury został przedstawiony na Ryc. 1.
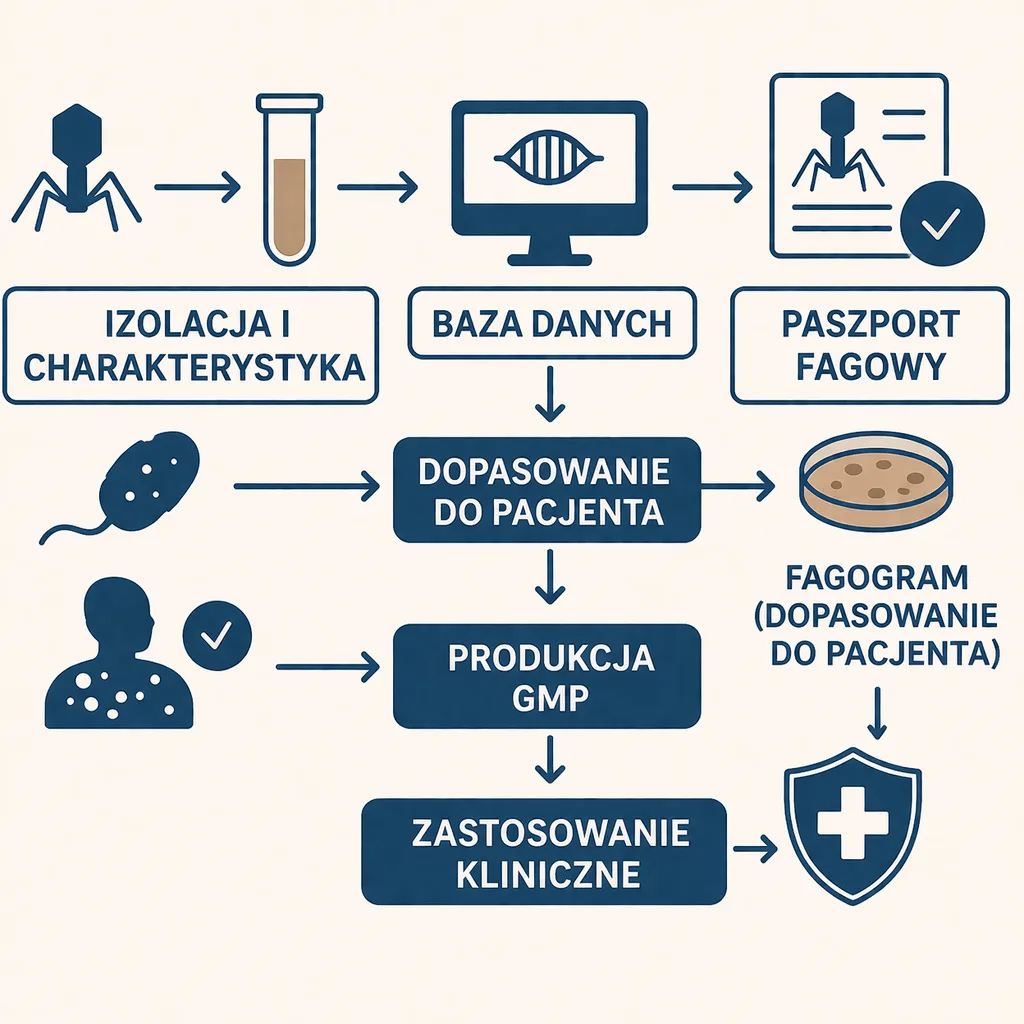
Podczas, gdy w Belgii, bądź Australii biobanki fagów działają jak dobrze zarządzana sieć, tak w wielu innych krajach nadal są to pojedyncze banki, które nie są ze sobą skomunikowane. Działają jak biblioteki fagów, nie mają standaryzowanego opisu [1, 5].
Początki kolekcji mikroorganizmów
Gwałtowny rozkwit oraz międzynarodowa współpraca organizacji, które tworzą kolekcje mikroorganizmów nastąpił po I Wojnie Światowej w krajach o wysokim dochodzie. Na przykład w 1920 r. powstała Narodowa Kolekcja Kultur Typowych (ang. National Collection of Type Cultures, NCTC) w Wielkiej Brytanii a 5 lat później w Stanach Zjednoczonych została założona Amerykańska Kolekcja Kultur Typowych (ang. American Type Culture Collection, ATCC). Także w Japonii powstało wiele przemysłowych i publicznych kolekcji kultur właśnie po to, by zintensyfikować wysiłki prowadzące do znalezienie, optymalizacji i zachowania wartościowych szczepów mikrobiologicznych [2]. Kolekcje, o których wspominam po dziś dzień istnieją i są głównymi kolekcjami skąd pozyskuje się nie tylko rożne szczepy bakterii, ale także eukariotyczne linie komórkowe [3, 4].
Był to czas, gdy świat już usłyszał o bakteriofagach i pojawiały się pierwsze doniesienia o ich użyteczności w terapii fagowej, natomiast nie były one na początku punktem zainteresowania kolekcji mikroorganizmów. Możliwe, że instytucje badawcze i medyczne nie wykazywały dużego zainteresowania kolekcjonowaniem fagów ze względu na kontrowersje, jakie wówczas narastały wokół fagów. Dotyczyło to niepewności, czy fagi są rzeczywiście wirusami, czy może enzymami. Dlatego też poszczególne fagi były kolekcjonowane i przechowywane w pojedynczych laboratoriach, które zajmowały się badaniem fagów. Nie było to w żaden sposób ustrukturyzowane i uporządkowane. W związku z tym nie było też żadnego ujednoliconego protokołu jak z fagami postępować, w tym jak je przechowywać, czy opisywać [2].
W ujednoliceniu protokółów dotyczących opisu, przechowywania, i dystrybucji międzynarodowych zestawów fagów referencyjncyh, to Międzynarodowy Komitet ds. Typowania Fagów Jelitowych jako pierwszy przetarł szlaki. Został on założony w 1947 r. i protokoły dotyczyły fagów jelitowych, jednak w ślad z nim zostały utworzone kolejne sieci typowania fagowego. Repozytoria fagowe także zaczęły powstawać w krajach Europy wschodniej i centralnej: Instytut Hirszfelda w Polsce, Niemieckim Wschodnim Centrum Epidemiologii Eksperymentalnej, Instytucie Eliavy w Gruzji i Moskiewskim Instytucie Gamalei w Rosji [2].
Jak powinny wyglądać biobanki fagów
Poza tym, że fagi powinny być odpowiednio przechowywane, to powinny tworzyć system zaprojektowany do podejmowania szybkich decyzji, zapewniać jakoś i jednorodność informacji. W Belgii stworzone są tzw. paszporty fagowe, które opisane są poniżej. Gdyby każdy bakteriofag, którego i tak się charakteryzuje byłby podobnie opisany ułatwiłoby to standaryzację danych, łatwość w ich odczycie i ich przekazywaniu, np. dla lekarzy.
Paszporty fagowe
Paszport bakteriofaga to jego unikalny identyfikator. Znajdują się tam ujednolicone metadane, które dotyczą podstawowych informacji o nim potrzebnych także do informacji. W paszporcie fagowym powinny znajdować się informacje, które są wylistowane poniżej [1, 6, 7].
- Identyfikacja i Metadane Podstawowe
- Unikalny identyfikator: Nazwa systemowa faga (np. zgodna ze standardami ICTV).
- Pochodzenie: Szczegółowe metadane kontekstowe (miejsce, data i źródło izolacji – np. ścieki miejskie, próbka kliniczna).
- Właściciel/Depozytariusz: Jednostka odpowiedzialna za utrzymanie szczepu w biobanku.
- Kwalifikacja Genomiczna (Fundament bezpieczeństwa)
- Pełna sekwencja genomu (WGS): Link do surowych danych i złożonego genomu.
- Analiza cyklu życiowego: Potwierdzenie braku genów odpowiedzialnych za lizogonię (wymagany wyłącznie cykl lityczny).
- Profil bezpieczeństwa: Certyfikat braku genów wirulencji, toksyn oraz markerów oporności na antybiotyki (AMR).
- Adnotacja funkcjonalna: Opis znanych sekwencji kodujących białka (CDS).
- Kwalifikacja Funkcjonalna (Profil działania)
- Zakres gospodarzy (Host Range): Lista specyficznych szczepów bakterii, na które fag działa (wraz z informacją o sile litycznej).
- Wydajność namnażania: Dane o kinetyce infekcji (np. czas adsorpcji, okres utajony).
- Stabilność: Informacje o odporności na czynniki zewnętrzne (np. pH, temperatura) istotne dla podania leku.
- Dane Operacyjne i Logistyczne
- Metoda konserwacji: Opis procedury przechowywania zapewniającej żywotność (np. liofilizacja, mrożenie).
- Czystość preparatu: Informacje o metodach oczyszczania (np. usuwanie endotoksyn).
- Zgodność regulacyjna: Status faga względem standardów (np. rozdział 5.31 Farmakopei Europejskiej).
- Historia i Aktualizacje (Dynamiczna Kuratela)
- Data ostatniej re-ewaluacji: Kiedy ostatnio sprawdzano skuteczność faga wobec ewoluujących szczepów bakterii.
- Historia użycia: (Jeśli dotyczy) Informacje o wcześniejszych sukcesach terapeutycznych lub badaniach in vivo [1, 6, 7].
Wyzwania w tworzeniu banków fagów
Tworzenie banków fagów wiąże się z licznymi wyzwaniami, szczególnie w krajach o ograniczonych zasobach. Choć lokalne ośrodki naukowe często posiadają kolekcje fagów skierowanych przeciwko endemicznym patogenom, problemem pozostaje dostęp do wysoko oczyszczonych preparatów spełniających standardy GMP, niezbędnych do zastosowań klinicznych, zwłaszcza dożylnego podania. Bariery finansowe i infrastrukturalne ograniczają rozwój produkcji oraz dystrybucji fagów na szeroką skalę. Dodatkowo, skuteczne funkcjonowanie biobanków wymaga solidnych ram prawnych, etycznych i organizacyjnych, a także stabilnych modeli finansowania. Wyzwanie stanowi również integracja działań z przemysłem oraz zapewnienie długoterminowej trwałości poprzez współpracę międzynarodową [1, 5, 8].
Publiczne finansowanie banków fagów
Czy dostęp do fagów, tak jak do antybiotyków powinien być finansowany publicznie? Czy powinny być refundowane? W Polsce terapia fagowa nadal jest terapią, która prawnie ma status eksperymentalnej, każdy kto jest zakwalifikowany do terapii musi za nią zapłacić z własnej kieszeni. Poniżej przedstawię kilka argumentów, które przemawiają za tym, żeby banki fagów uwzględnić, przynajmniej częściowo, w publicznym finansowaniu.
1. Banki fagów jako „dobro publiczne”
Zgodnie z tekstem, istnieje silny argument za wspieraniem banków fagów z funduszy publicznych, ponieważ służą one całemu społeczeństwu. Społeczność wierzy, że wysokiej jakości kolekcje okazów biologicznych znacząco przyspieszają innowacje i rozwój badań biomedycznych.
2. Walka z antybiotykoopornością (AMR)
Koszty opieki zdrowotnej związanej z infekcjami lekoopornymi stale rosną. Publiczne finansowanie infrastruktury fagowej jest formą prewencji – inwestycja w alternatywne terapie teraz może zapobiec astronomicznym kosztom dłuższego leczenia i hospitalizacji pacjentów w przyszłości.
3. Demokratyzacja dostępu do leczenia
W krajach rozwijających się, gdzie problem antybiotykooporności jest najdotkliwszy, publiczne wsparcie pozwala na:
- drastyczne obniżenie cen preparatów,
- wyrównanie szans w dostępie do nowoczesnych terapii,
- lokalną produkcję fagów, co uniezależnia te kraje od drogiego importu leków.
4. Zapewnienie bezpieczeństwa i standardów (GMP)
Prywatne, rozproszone inicjatywy często nie mają środków na oczyszczanie ze standardami GMP (Dobrej Praktyki Wytwarzania). Państwowe finansowanie pozwala na budowę profesjonalnych centrów oczyszczania fagów, co gwarantuje bezpieczeństwo pacjentów (szczególnie przy podawaniu dożylnym).
5. Stabilność w obliczu mechanizmów rynkowych
Banki biologiczne rzadko są rentowne w krótkim terminie (często wykazują niskie początkowe wykorzystanie zbiorów). Publiczna dotacja zapewnia im przetrwanie w okresach niskich wpływów komercyjnych, chroniąc cenne kolekcje przed likwidacją.
6. Infrastruktura dla nauki i przemysłu
Dobrze sfinansowany bank to nie tylko magazyn, ale inteligentna platforma ułatwiająca:
- szybkie dopasowywanie fagów do konkretnych szczepów bakterii pacjenta (personalized therapy),
- współpracę z firmami biotech i pharma, które mogą szybciej wdrażać nowe leki dzięki gotowym zasobom banku [1, 2, 5, 8].
Podsumowanie
W dobie narastającej lekooporności bakterii zastosowanie bakteriofagów już nie tylko jako tarapia eksperymentalna wydaje się być coraz bardziej realnym scenariuszem. Powinniśmy zacząć się do tego przygotowywać, m. in. poprzez wykonanie infrastruktury służącej do dystrybucji fagów w każdym zakątku świata, ale zaczynając od własnego kraju. Biobanki fagów, powinny być czymś więcej niż tylko magazynem próbek. Biorąc przykład z Belgii można stworzyć wspólną dla każdego procedurę, w którym każdy będzie poruszać się z łatwością, dzięki czemu pacjenci szybciej otrzymają swoją terapię i zostaną wyleczeni.
Literatura
- Topa-Pila P, Morales KY, Palacios-Mora DP, Flores-Hernández C, Altamirano-Cisneros A, Gavilanes JM, Villacís-López K, Arancibia M, Mora-Domínguez J, Calero-Cáceres W. Phage biobanks as enabling infrastructure for precision phage therapy in the era of antimicrobial resistance. Front Antibiot. 2026 Jan 30;5:1772871. DOI:10.3389/frabi.2026.1772871.
- Resch G, Brives C, Debarbieux L, Hodges FE, Kirchhelle C, Laurent F, Moineau S, Martins AFM, Rohde C. Between Centralization and Fragmentation: The Past, Present, and Future of Phage Collections. Phage (New Rochelle). 2024 Mar 18;5(1):22-29. DOI:10.1089/phage.2023.0043.
- https://www.atcc.org/
- https://www.culturecollections.org.uk/about-us/nctc/
- Lin, R. C., Sacher, J. C., Ceyssens, P. J., Zheng, J., Khalid, A., Iredell, J. R., & Network, T. A. P. B. (2021). Phage biobank: present challenges and future perspectives. Current opinion in biotechnology, 68, 221-230. DOI:10.1016/j.copbio.2020.12.018.
- Djebara, S., Maussen, C., De Vos, D., Merabishvili, M., Damanet, B., Pang, K. W., … & Pirnay, J. P. (2019). Processing phage therapy requests in a Brussels military hospital: Lessons identified. Viruses 11. DOI:10.3390/v11030265
- Pirnay, J. P., & Verbeken, G. (2023). Magistral phage preparations: is this the model for everyone?. Clinical Infectious Diseases, 77(Supplement_5), S360-S369. DOI:10.1093/cid/ciad481
- Xing, B., Liu, C., Chen, W. et al. Gut Phage Biobank: a collection of bacteriophages targeting human commensal bacteria. Nat Commun 16, 11050 (2025). DOI:10.1038/s41467-025-61946-0
