Bakteriofagi mogą być izolowane z każdej powierzchni, np. telefonu komórkowego, banknotów, umywalki w toalecie, czy płynu, jak ścieki komunalne, albo woda z jeziora. Fagi wykorzystywane w terapii zwykle kolekcjonuje się izolując je ze ścieków szpitalnych, gdzie izolować się będzie fagi zjadliwe dla bakterii patogennych, jakie chcemy zwalczać. Takie bakteriofagi trzeba najpierw odpowiednio przygotować, by móc podać je pacjentom i w tym artykule skupimy się głównie na ostatnim kroku, czyli oczyszczaniu.
Spis treści
Główne kroki w przygotowaniu preparatu bakteriofagowego
W produkcji fagów można wyróżnić 3 główne kroki:
- namnożenie fagów,
- zagęszczenie fagów,
- oczyszczanie fagów.
W terapii fagowej powinno się wykorzystywać fagi, które są przede wszystkim zjadliwe wobec patogenu, ale istnieje kilka czynników/warunków jakie należy określić, aby fagi namnożyć jak najbardziej efektywnie. Należy je dobrze scharakteryzować pod kątem plonu fagowego (ile fagów wydostanie się z komórek bakteryjnych po jednym cyklu), adsorpcję do powierzchni komórki gospodarza (jak szybko i efektywnie fag rozpoznaje komórkę bakteryjną oraz „przyczepia się” do jej powierzchni) oraz wielokrotność zakażenia (ang. Multiplicity Of Infection, MOI – stosunek ilości komórek bakterii do faga, np. 0,1 oznacza, że na 10 komórek bakteryjnych przypada 1 bakteriofag, a MOI 10 oznacza 10 cząsteczek wirusa przypadających na 1 komórkę bakteryjną) [1, 2, 3].
Oczyszczenie bakteriofagów
Namnażanie
Bakteriofagi namnaża się w bakteriach. Wykorzystuje się ich naturalną zdolność do infekowania komórek bakteryjnych, w których potem fagi wykorzystują maszynerię replikacyjną gospodarza do produkcji wirionów potomnych, które po złożeniu uwalniane są do środowiska w wyniku lizy bakterii i mogą powtórzyć cykl od początku [1]. Hodowlę bakteryjną infekuje się fagami zazwyczaj w momencie, gdy bakterie zaczynają wchodzić w fazę wzrostu logarytmicznego [1, 2]. Fagi produkuje się by uzyskać jak najwyższe miano i zazwyczaj do momentu, gdy pożywka mikrobiologiczna jest prawie przejrzysta. Obserwuje się wtedy też tzw. kłaczki, czyli drobne, cienkie, białe niteczki.
Oddzielenie bakteriofagów od bakterii
Po zakończeniu lizy surowy lizat zawiera szczątki komórek bakteryjnych. Wstępne oczyszczanie polega na usuwaniu resztek bakteryjnych poprzez wirowanie oraz filtrację membranową (zwykle filtry 0,22 µm), co pozwala uzyskać klarowny roztwór zawierający wolne fagi [2, 5].
W takiej hodowli pozostają resztki bakteryjne takie jak: endotoksyny, egzotoksyny, peptydoglikan, kwasy nukleinowe, itp. Są to toksyny dla naszych organizmów i mogą doprowadzić do ciężkiego stanu zapalnego a nawet do sepsy.
Dlatego istnieje kilka metod, które pomogą nam fagi oczyścić. Można wykorzystać:
- filtrowanie przez filtry o wielkości porów 0,22 – 0,45 µm [2, 5],
- rozpuszczalniki organiczne jak chloroform (chociaż nie wszystkie fagi są odporne na działanie chloroformu) [1],
- precypitację glikolem polietylenowym (PEG), gdzie dochodzi do zagęszczenia fagów poprzez ich wytrącenie z roztworu [2],
- ultrawirowanie w gradiencie gęstości chlorku cezu (CsCl) bądź sacharozy – nie wszystkie fagi są odporne na chlorek cezu [2],
- ultrafiltrację i filtrację styczną [4],
- chromatografię cieczową [4].
Podczas przygotowania lizatu fagowego łączy się ze sobą te metody w poszczególne etapy. Styczna filtracja przepływowa i chromatografia cieczowa to nowsze metody, które stosuje coraz częściej. Są one lepsze od PEGu i CsCl, który często doprowadza do mniejszego odzysku fagów z powodu ich inaktywacji podczas zagęszczania.
Precipitacja z użyciem PEG (polietylenoglikolu)
Precipitacja z użyciem polietylenoglikolu (PEG) jest jedną z najczęściej stosowanych metod koncentracji bakteriofagów na etapie wstępnego oczyszczania. Proces polega na dodaniu do lizatu bakteryjnego PEG (najczęściej PEG 8000) oraz soli, zwykle NaCl. Zwiększona siła jonowa i obecność PEG powodują zmniejszenie rozpuszczalności cząstek fagowych, co prowadzi do ich agregacji i wytrącania z roztworu [2]. Po inkubacji w niskiej temperaturze mieszaninę poddaje się wirowaniu, w wyniku czego powstaje osad zawierający skoncentrowane cząstki fagowe. Następnie osad jest zawieszany w odpowiednim buforze. Metoda ta jest stosunkowo prosta, tania i pozwala na jednoczesne przetwarzanie dużych objętości lizatu. Jej ograniczeniem jest jednak współprecypitacja białek gospodarza i innych zanieczyszczeń, dlatego zwykle stanowi jedynie etap przygotowawczy przed dalszym oczyszczaniem. Dodatkowo wykazano, że standardowe procedury precypitacji mogą prowadzić do częściowej utraty liczby cząstek fagowych lub obniżenia ich aktywności biologicznej [5].
Ultrawirowanie w gradiencie gęstości (CsCl)
Ultrawirowanie w gradiencie chlorku cezu (CsCl) jest jedną z najbardziej klasycznych metod uzyskiwania wysokooczyszczonych preparatów bakteriofagowych. Technika ta wykorzystuje różnice w gęstości cząstek obecnych w próbce (schemat przedstawiający nałożenie gradientu CsCl oraz sacharozy do probówki znajduje się na Ryc. 1).
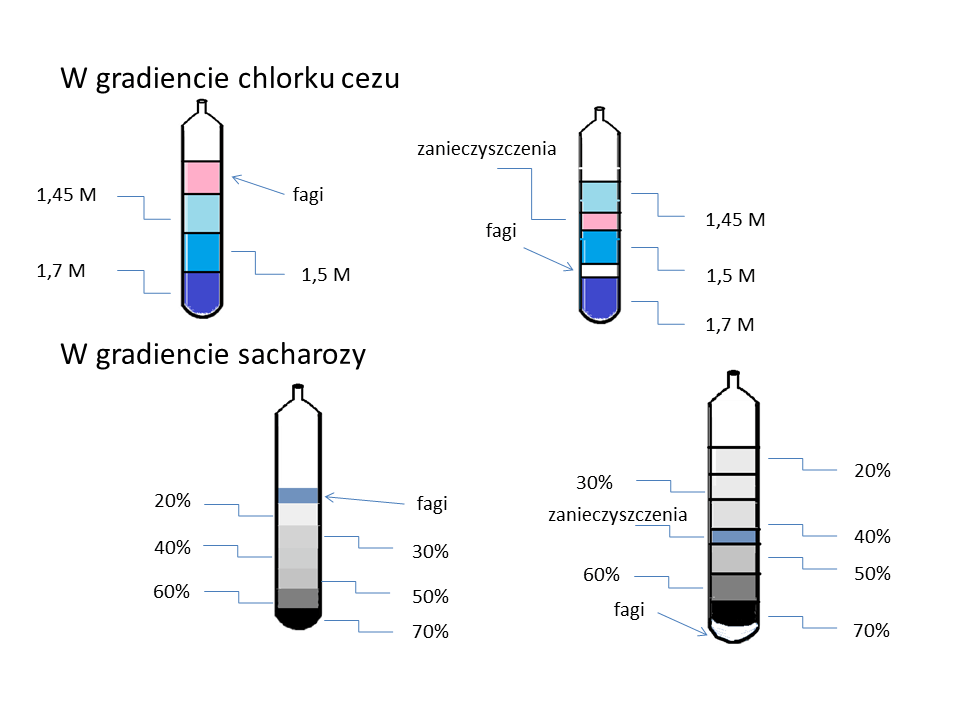
Przygotowany gradient CsCl poddaje się ultrawirowaniu, co powoduje powstanie stabilnego gradientu gęstości. W trakcie wirowania cząstki fagowe migrują do warstwy o gęstości odpowiadającej ich własnej gęstości izopiknicznej [2]. Dzięki temu możliwe jest oddzielenie fagów od białek bakteryjnych, fragmentów komórkowych oraz innych cząstek biologicznych. Po zakończeniu wirowania widoczny jest charakterystyczny pas fagowy, który można pobrać za pomocą igły lub pipety. Następnie konieczne jest usunięcie CsCl, zwykle poprzez dializę lub ultrafiltrację. Metoda ta zapewnia bardzo wysoką czystość preparatu i jest szeroko stosowana w badaniach laboratoryjnych. Jej wadą jest jednak czasochłonność, konieczność użycia ultrawirówki oraz możliwość obniżenia stabilności niektórych fagów podczas ekspozycji na wysokie siły odśrodkowe i wysokie stężenia soli [2, 3]. Na Ryc. 2., która została zaczęrpnięta z artykułu Carroll-Portillo i in. [5] można zobaczyć różnicę w czystości preparatu do PEGu oraz CsCl.
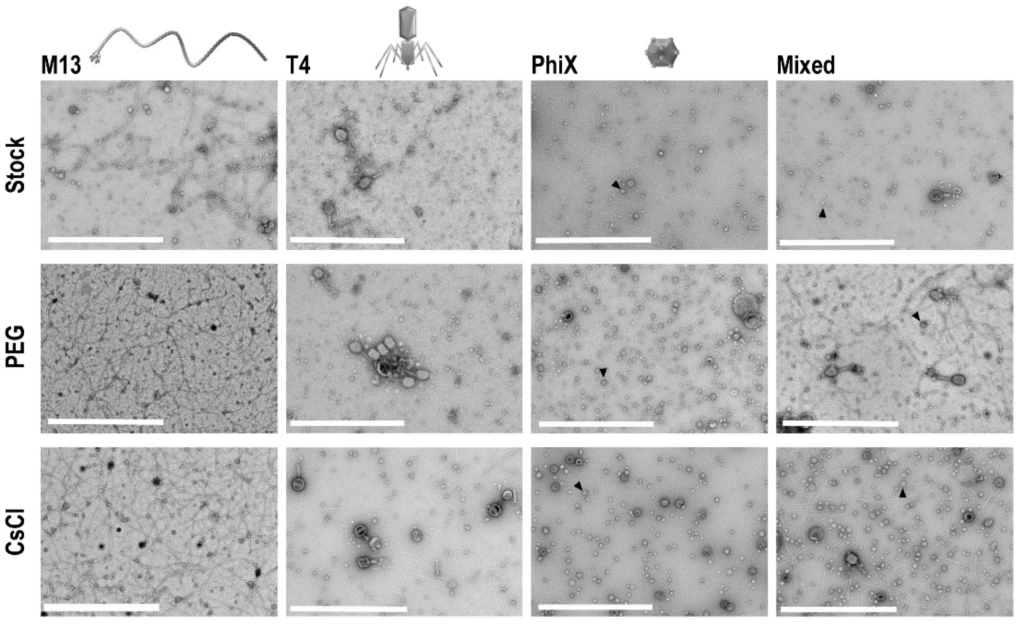
Ultrafiltracja i filtracja styczna (TFF)
Ultrafiltracja jest techniką membranową wykorzystywaną do zagęszczania bakteriofagów oraz usuwania drobnocząsteczkowych zanieczyszczeń. W metodzie tej próbkę przepuszcza się przez membranę o określonym progu odcięcia masy cząsteczkowej (ang. Molecular Weight Cut Off, MWCO), która zatrzymuje cząstki fagowe, a przepuszcza mniejsze cząsteczki, takie jak sole, metabolity czy drobne białka [4]. Szczególną odmianą tej techniki jest filtracja styczna (ang. Tangential Flow Filtration, TFF), w której przepływ cieczy odbywa się równolegle do powierzchni membrany. Taki układ ogranicza zatykanie membrany i pozwala na przetwarzanie dużych objętości materiału biologicznego. TFF umożliwia jednocześnie koncentrację fagów oraz wymianę buforu (diafiltrację), co jest istotne w przygotowaniu preparatów przeznaczonych do zastosowań terapeutycznych. Metoda ta jest skalowalna i stosowana w procesach produkcyjnych, ponieważ pozwala na stosunkowo łagodne traktowanie cząstek fagowych i zachowanie ich aktywności biologicznej. Jednak skuteczność procesu zależy od odpowiedniego doboru membrany i parametrów przepływu [4].
Chromatografia (np. jonowymienna)
Chromatografia jest jedną z najbardziej zaawansowanych metod oczyszczania bakteriofagów i znajduje zastosowanie szczególnie w produkcji preparatów o wysokim stopniu czystości. W chromatografii jonowymiennej rozdział opiera się na różnicach w ładunku powierzchniowym cząstek fagowych oraz zanieczyszczeń obecnych w lizacie. Kolumna chromatograficzna zawiera złoże z naładowanymi grupami funkcyjnymi, które wiążą cząstki o przeciwnym ładunku [4]. Po wprowadzeniu próbki zanieczyszczenia mogą być wypłukiwane z kolumny, natomiast bakteriofagi pozostają związane z fazą stacjonarną lub odwrotnie – w zależności od konfiguracji systemu. Następnie fagi eluowane są przy użyciu gradientu soli lub zmian pH. Technika ta umożliwia skuteczne usuwanie białek gospodarza, endotoksyn oraz innych zanieczyszczeń biologicznych. Chromatografia jest dobrze skalowalna, dlatego jest preferowana w produkcji komercyjnej (standardy GMP) i może być integrowana z innymi metodami oczyszczania, np. ultrafiltracją. Jej wadą jest jednak wyższy koszt aparatury i konieczność optymalizacji warunków separacji dla każdego typu bakteriofaga [4].
Nowoczesne metody i wyzwania
Współczesna terapia fagowa dąży do standaryzacji protokołów (np. zrobotyzowane platformy oczyszczania), aby umożliwić szybkie przygotowanie spersonalizowanych koktajli [2]. Wyzwaniem pozostaje fakt, że standardowe procedury mogą powodować znaczne straty w liczbie i aktywności faga [5]. Stabilność faga zależy od pH, temperatury oraz składu buforów użytych podczas oczyszczania [3].
Podsumowanie
Skuteczność terapii fagowej zależy nie tylko od doboru faga, ale od czystości i stabilności preparatu. Wybór metody oczyszczania musi balansować między wysoką wydajnością a zachowaniem biologicznej aktywności wirusów [1, 4].
Literatura
- Sippel, K., & Velimirov, B. (2025). Phage Therapy: Application and Related Problems—A Review. Life, 16(1), 57. DOI:10.3390/life16010057
- Luong, T., Salabarria, AC., Edwards, R.A. et al. Standardized bacteriophage purification for personalized phage therapy. Nat Protoc 15, 2867–2890 (2020). https://doi.org/10.1038/s41596-020-0346-0
- Jończyk-Matysiak, E., Łodej, N., Kula, D., Owczarek, B., Orwat, F., Międzybrodzki, R., … Górski, A. (2019). Factors determining phage stability/activity: challenges in practical phage application. Expert Review of Anti-Infective Therapy, 17(8), 583–606. https://doi.org/10.1080/14787210.2019.1646126
- Malik, D. J. (2021). Approaches for manufacture, formulation, targeted delivery and controlled release of phage-based therapeutics. Current opinion in biotechnology, 68, 262-271. doi.org/10.1016/j.copbio.2021.02.009
- Carroll-Portillo, A., Coffman, C. N., Varga, M. G., Alcock, J., Singh, S. B., & Lin, H. C. (2021). Standard bacteriophage purification procedures cause loss in numbers and activity. Viruses, 13(2), 328. https://doi.org/10.3390/v13020328
