Bakteriofagi dostarczane są pacjentowi na ranę, doustnie, poprzez inhalację, czy do krwiobiegu. Jaka droga podania bakteriofagów jest najlepsza? W jakiej postaci bakteriofagi podawać najlepiej? Postaram się przybliżyć te zagadnienia w poniższym artykule z tego, co wiemy na dzień dzisiejszy.
Drogi podania bakteriofagów
Terapia fagowa jest przykładem terapii personalizowanej, co oznacza, że trzeba ją odpowiednio dobrać dla danego pacjenta. Droga podania bakteriofagów pacjentowi dobierana jest do zapotrzebowań pacjenta i miejsca infekcji [1].
Drogi podawania bakteriofagów pacjentów możemy podzielić na dwie główne grupy: podanie systemowe i podanie lokalne [1, 2].
Podanie systemowe to podanie:
- dożylne,
- doustne,
- dootrzewnowe (bezpośrednio przez układ pokarmowy).
Podanie lokalne:
- Miejscowe – w przypadku zakażeń skórnych,
- Do oka, nosa, ucha – w formie kropli,
- Inhalacje, nebulizacje – w przypadku infekcji układu oddechowego,
- bezpośrednio do stawów – w przypadku zakażeń stawów protetycznych,
- do pęcherza moczowego – w przypadku zakażeń układu moczowego.
Badania pokazują, że podanie lokalne może wymagać użycia wyższego stężenia fagów niż podanie dożylne [1]. Na Ryc.1. znajdują się przykładowe drogi podania bakteriofagów.
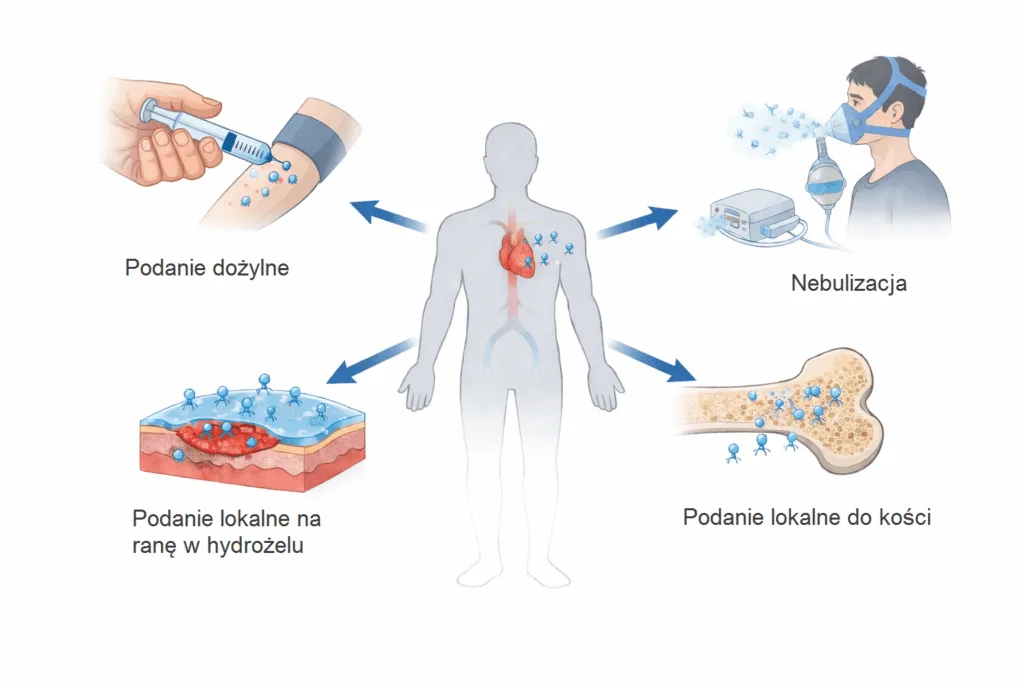
Drogi podania bakteriofagów i ich szczegółowy opis
Wybór metody aplikacji faga jest determinowany przez: typ i farmakokinetykę wirusa, czyli to, jak szybko jest on usuwany z organizmu oraz czy jest w stanie przeniknąć do specyficznej tkanki, np. kości czy płuc [1, 3].
Podanie ogólnoustrojowe
Jest to preferowana metoda w przypadku zakażeń układowych, sepsy oraz infekcji głęboko osadzonych w narządach wewnętrznych. Podanie dożylne zapewnia natychmiastową dystrybucję cząstek fagowych w całym krwiobiegu, co teoretycznie pozwala na dotarcie do każdego zainfekowanego miejsca w organizmie. Jednakże, fagi jako cząstki białkowe są traktowane przez organizm jako elementy obce i podlegają szybkiej filtracji oraz neutralizacji przez układ siateczkowo-śródbłonkowy, głównie w wątrobie i śledzionie. Powoduje to krótki okres półtrwania faga w surowicy, co wymusza stosowanie częstych dawek (np. co 6, 8 lub 12 godzin) lub wlewu ciągłego, aby utrzymać stężenie wirusów powyżej progu niezbędnego do replikacji na bakteriach. Dodatkowym aspektem jest monitoring immunologiczny, gdyż przy długotrwałej terapii systemowej organizm może wytworzyć przeciwciała neutralizujące fagi. Mimo tych wyzwań, podanie dożylne jest kluczowe w stanach krytycznych, gdzie konieczna jest szybka interwencja przeciwko patogenom takim jak Staphylococcus aureus czy Acinetobacter baumannii bytującym w łożysku naczyniowym. Precyzyjne oczyszczenie preparatu jest w tej metodzie absolutnie krytyczne, aby uniknąć wstrząsu endotoksycznego [1].
Przykład pacjenta (podanie dożylne)
W literaturze udokumentowano przypadek pacjenta zmagającego się z rozsianą, zagrażającą życiu infekcją wywołaną przez wielolekooporny szczep Acinetobacter baumannii. Po niepowodzeniu standardowej antybiotykoterapii, zespół medyczny zdecydował się na wdrożenie personalizowanej terapii fagowej drogą dożylną. Preparat był podawany w formie cyklicznych wlewów, co miało na celu nasycenie łożyska naczyniowego i skompensowanie naturalnej eliminacji wirusów przez wątrobę i śledzionę pacjenta. Podczas całego procesu monitorowano parametry zapalne oraz miano fagów we krwi, aby upewnić się, że wirusy skutecznie infekują komórki bakteryjne. Terapia doprowadziła do wyraźnej poprawy klinicznej i ostatecznego wyeliminowania patogenu z krwiobiegu. Co istotne, w trakcie leczenia zaobserwowano zjawisko zwiększenia wrażliwości bakterii na antybiotyki, co pozwoliło na skuteczne zakończenie kuracji metodą skojarzoną. Pacjent powrócił do zdrowia bez wystąpienia poważnych zdarzeń niepożądanych, co potwierdziło bezpieczeństwo rygorystycznie oczyszczonych preparatów dożylnych w sytuacjach ratunkowych [4].
Podanie lokalne i celowane
Podanie lokalne polega na bezpośredniej aplikacji leku do miejsca infekcji, co pozwala na zastosowanie dawek wielokrotnie przekraczających bezpieczne stężenia ogólnoustrojowe [2, 3].
Nebulizacja i zakażenia układu oddechowego
Podawanie fagi i enzymów drogą wziewną (nebulizacja) jest kluczowe w leczeniu przewlekłych zakażeń płuc, np. u pacjentów z mukowiscydozą. Metoda ta pozwala na bezpośrednie dotarcie wirusów do biofilmu bakteryjnego w drogach oddechowych, omijając barierę krew-płuco, która często ogranicza skuteczność antybiotyków podawanych dożylnie. Fagi dostarczane w formie aerozolu mogą skutecznie redukować populację Pseudomonas aeruginosa bez wywoływania ogólnoustrojowych skutków ubocznych [1].
Zakażenia układu moczowego
W przypadku zakażeń pęcherza moczowego terapeutyki mogą być podawane poprzez bezpośrednie cewnikowanie (płukanie pęcherza). Jest to szczególnie skuteczne w zwalczaniu bakterii wielolekoopornych, które kolonizują cewniki moczowe. Dzięki bezpośredniej aplikacji fagi mogą niszczyć biofilm na powierzchniach sztucznych materiałów, co jest niemal niemożliwe przy tradycyjnym leczeniu doustnym ze względu na niskie stężenie leków w moczu [1].
Leczenie ran przewlekłych i hydrożele
W leczeniu zainfekowanych ran (np. stopy cukrzycowej) stosuje się nowoczesne hydrożele, takie jak system „HydroPhage”. Zamiast gwałtownego wyrzutu leku, oferują one stałe uwalnianie fagów przez ponad 7 dni. Hydrożele te, oparte na kwasie hialuronowym, zapewniają wilgotne środowisko sprzyjające gojeniu, jednocześnie chroniąc fagi przed wysychaniem i dezaktywacją przez enzymy tkankowe [2].
Zapalenie kości, stawów i cementy kostne
W ortopedii terapeutyki dostarcza się poprzez cementy kostne obciążone lekami oraz wstrzykiwalne materiały kompozytowe. Pozwala to na penetrację skomplikowanych struktur kości, gdzie bakterie ukrywają się przed układem odpornościowym [3]. Stosuje się tu również biodegradowalne gąbki kolagenowe oraz wstrzykiwalne hydrożele dostarczające lizostafinę bezpośrednio do ubytków kostnych, co minimalizuje ryzyko nawrotu infekcji po operacji [3].
Przykład pacjentów (podanie lokalne):
Rozważmy modelowy przypadek pacjenta z przewlekłym zapaleniem kości po wszczepieniu implantu. Tradycyjne płukanie rany antybiotykami nie przyniosło efektu z powodu obecności biofilmu gronkowca. Zastosowanie miejscowe hydrożelu nasyconego lizostafiną lub specyficznymi fagami bezpośrednio podczas chirurgicznego oczyszczania tkanki pozwoliło na całkowitą eliminację patogenu. W przeciwieństwie do pacjentów leczonych tylko ogólnoustrojowo, u osób z aplikacją lokalną odnotowano znaczną poprawę w procesie gojenia kości i rekonstrukcji tkanek. Badania przedkliniczne potwierdzają, że lokalne dostarczanie fagów za pomocą systemów hydrożelowych lub gąbek kolagenowych zapewnia wysoką skuteczność eradykacji bakterii, chroniąc jednocześnie pacjenta przed toksycznością wysokich dawek leków we krwi [1, 2, 3].
Wyzwania i perspektywy
Kluczowym problemem pozostaje opracowanie ustandaryzowanych protokołów dawkowania. Przyszłość leży w terapiach skojarzonych oraz w wykorzystaniu „inteligentnych” nośników reagujących na obecność bakterii, na przykład rozkładających się pod wpływem substancji wydzielanych przez konkretne szczepy patogenów [3].
Podsumowanie
Efektywna terapia infekcji lekoopornych wymaga odejścia od wyłącznie ogólnoustrojowego podawania leków na rzecz zaawansowanych metod lokalnych. Hydrożele o przedłużonym uwalnianiu, nebulizacja oraz spersonalizowane nośniki kostne stanowią przełom, pozwalając na precyzyjne uderzenie w biofilm przy zachowaniu pełnego bezpieczeństwa pacjenta [1, 2, 3].
Literatura
- Kim, M. K., Suh, G. A., Cullen, G. D., Rodriguez, S. P., Dharmaraj, T., Chang, T. H. W., … & Sacher, J. C. (2025). Bacteriophage therapy for multidrug-resistant infections: current technologies and therapeutic approaches. The Journal of Clinical Investigation, 135(5). DOI:10.1172/JCI187996.
- Lin, Y. H., Dharmaraj, T., Chen, Q., Echterhof, A., Manasherob, R., Zheng, L. J., … & Bollyky, P. (2024). Hydrogels for local and sustained delivery of bacteriophages to treat multidrug-resistant wound infections. bioRxiv, 2024-05.DOI.org/10.1101/2024.05.07.593005
- Cobb, L. H., McCabe, E. M., & Priddy, L. B. (2020). Therapeutics and delivery vehicles for local treatment of osteomyelitis. Journal of Orthopaedic Research®, 38(10), 2091-2103. DOI:10.1002/jor.24689
- Schooley, R. T., Biswas, B., Gill, J. J., Hernandez-Morales, A., Lancaster, J., Lessor, L., … & Hamilton, T. (2017). Development and use of personalized bacteriophage-based therapeutic cocktails to treat a patient with a disseminated resistant Acinetobacter baumannii infection. Antimicrobial agents and chemotherapy, 61(10), 10-1128. DOI:10.1128/aac.00954
